
全世界大概有200萬人需要器官移植,但是器官捐獻的數量遠遠低於需要的人數。
移植器官供體不足隨著老齡化和慢性疾病的多發而愈發嚴重。
豬的器官因為大小和功能和人類似,被認為是最有可能成為能移植到人的異種器官。
上世紀90年代,歐美政府花大力氣來推動豬器官移植項目,
幾個全球大藥廠也投了巨資希望解決豬器官的人體排斥問題,
但沒想到後來發現豬的基因組裡面有內源性逆轉錄病毒存在,
最終世界衛生組織和美國政府都明令,
在找到解決辦法之前,停止一切異種器官移植的臨床試驗。
內源性逆轉錄病毒是嵌在細胞內基因組的病毒,在豬身體裡面不會有毒性。
但當豬的細胞和人的細胞接觸時,這種病毒會從豬的基因組「跳」到人的基因組中。
異種病毒傳播最典型的例子就是愛滋病病毒(一種逆轉錄病毒)
從靈長類動物傳播到人類,至今還沒有有效徹底的醫療方法防禦和清除愛滋病毒。
因此,豬基因組的內源性逆轉錄病毒成為人體移植利用豬器官面臨的一個重大醫療風險問題。

楊璐菡與她在哈佛博士生導師合作,利用新基因編輯技術敲除豬基因組中可能致病基因
美國哈佛大學和生物技術公司eGenesis研究人員最近利用一種新的基因編輯技術,
敲除了豬基因組中可能有害的病毒基因,
從而掃清豬器官用於人體移植的重大難關,
為全世界亟需器官移植的上百萬病人帶來希望。
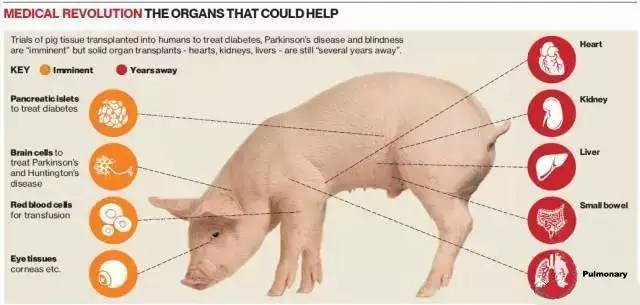
重燃異種器官移植信心
鑒於這項成果的意義重大,美國《科學》雜誌一次性審稿,並提前在線刊登論文。
哈佛大學和eGenesis異種器官移植課題帶頭人楊璐菡告訴記者:
「這個工作掃除了10多年前發現豬內源性逆轉錄病毒後在這個領域的最大的安全障礙,
也重新燃起了大家對異種器官移植的信心。」
內源性逆轉錄病毒是嵌在細胞內基因組的病毒,在豬身體裡面不會有毒性。
但當豬的細胞和人的細胞接觸時,這種病毒會從豬的基因組「跳」到人的基因組中。
異種病毒傳播最典型的例子就是愛滋病病毒從靈長類動物傳播到人類。
因此,豬基因組的內源性逆轉錄病毒成為人體移植利用豬器官面臨的一個重大醫療風險問題。
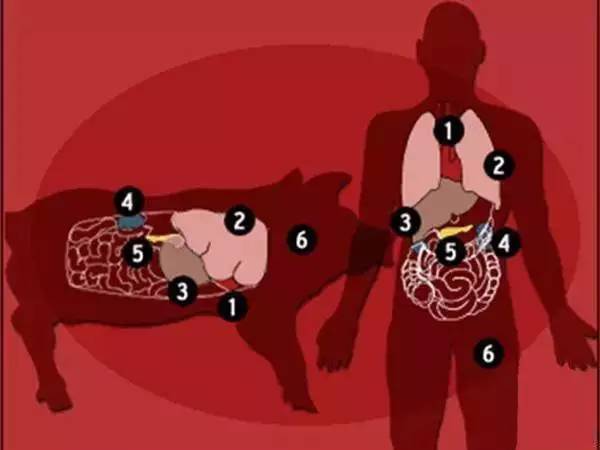
豬病毒侵染率大幅下降
楊璐菡和她在哈佛的博士生導師、美國科學院及工程學院雙料院士喬治·丘奇創立了一家叫eGenesis的生物技術公司,致力於推動異種器官移植臨床應用。
從2014年起,楊璐菡作為異種器官移植課題帶頭人,
帶領10個人的科研團隊在哈佛和eGenesis利用新發明的一種叫做CRISPR-Cas9的「基因剪刀」技術,敲除豬基因組中可能的致病基因。
當丘奇和楊璐菡改造後的豬細胞和人的細胞一起培養時,
他們發現,豬病毒「侵染率下降到了至少以前的1/1000」,
「在監測靈敏度範圍內檢測不到任何侵染」。

今年29歲的楊璐菡2008年本科畢業於北京大學,
曾因第一個利用CRISPR-Cas9技術修改細胞基因組和領導eGenesis,
而被福布斯雜誌評為2014年30歲以下30個科學醫療領域(30 under 30)領軍人物之一。
她說,希望在接下來5年時間內,把異種器官移植向臨床方向推動。
當然,異種器官移植除了技術方面的問題,還有生物倫理問題、商業規範問題等需要解決。
|